Urolitin A(veza:https://www.bloomtechz.com/synthetic-chemical/api-researching-only/urolithin-a-powder-cas-1143-70-0.html), engleski naziv Urolithin A, je žuti ili svijetložuti čvrsti prah pri normalnoj temperaturi i pritisku. Urolitin A je intestinalni mikrobni metabolit elaginske kiseline, koji ima protuupalna, antiproliferativna i antioksidativna svojstva, a može se koristiti kao organska sinteza, biohemijski intermedijeri i biološki reagensi stanica, a može se primijeniti na molekule lijekova i bioaktivan modifikacija i derivatizacija molekula. Urolitin A se može rastvoriti u jakim polarnim organskim rastvaračima kao što su dimetil sulfoksid, N,N-dimetilformamid, ali je slabo rastvorljiv u petroleteru niskog polariteta i dietil etru, a takođe je rastvorljiv u vodi. veoma loše. Urolitin A je intestinalni metabolit elaginske kiseline sa antioksidativnim i antiproliferativnim efektima; vrijednosti IC50 za inhibiciju rasta T24 i Caco{7}} ćelija bile su 43,9 i 49 μM, respektivno, a urolitin A može uglavnom inhibirati rak prostate i rast ćelija raka debelog crijeva.
Urolitin A (Urolithin A) je prirodna bioaktivna supstanca koja ima različite zdravstvene prednosti kao što su antioksidacija, anti-inflamacija i anti-mišićna atrofija.
Prva metoda su specifični koraci i hemijske jednačine sinteze urolitina A upotrebom prekursora urolitina A i AlCl3.
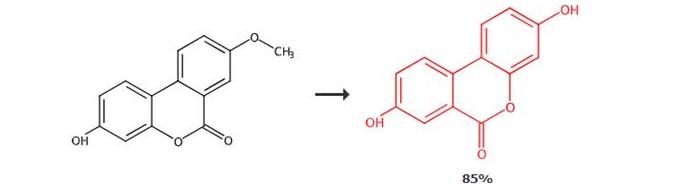
Korak 1: Sinteza prekursora urolitina A
Hrastova kiselina plus H2O plus kiselo stanje → prekursor urolitina A
Prekursorska jedinjenja urolitina A mogu se dobiti različitim sintetičkim putevima, jedna od tipičnih metoda je izlaganje prirodnih polifenolnih jedinjenja (kao što je hrastova kiselina u hrastovoj kori) u biljkama kiseloj hidrolizi, reakcijama oksidacije i acilacije, itd. Koraci Sinteza Prekursor urolitina A.
Korak 2: Reakcija kondenzacije prekursora urolitina A sa AlCl3
Prekursor urolitina A plus AlCl3→ proizvod kondenzacije
Prekursorsko jedinjenje urolitina A dobijeno u koraku 1 kondenzuje se sa aluminijum trihloridom (AlCl3) pod odgovarajućim rastvaračem i uslovima. Ova reakcija se obično mora provesti u inertnoj atmosferi, kao što je atmosfera dušika, kako bi se spriječile reakcije oksidacije.
Korak 3: Kisela hidroliza
Proizvod kondenzacije plus HCl plus H2O → urolitin A
Produkt kondenzacije dobijen u koraku 2 podvrgava se kiseloj hidrolizi, na primjer, razrijeđena hlorovodonična kiselina (HCl) se koristi za hidrolizu u kiselim uslovima. Ovaj korak može hidrolizirati estersku vezu u produktu kondenzacije kako bi se stvorila struktura urolitina A.
Korak 4: Kristalizacija i pročišćavanje
Nakon kisele hidrolize, urolitin A se taloži u kristalnom obliku. Proizvod urolitina A veće čistoće može se dobiti izvođenjem odgovarajućih operacija ispiranja i prečišćavanja rastvaračem.
Druga metoda je refluksiranje mješavine {{0}}bromo-5-hidroksibenzojeve kiseline (0,5 g, 2,3 mmol) i resorcinola (1,5 g, 13,8 mmol) u 16,8 mmol vodenog rastvora NaOH (25 mL) ) tokom 1 h, a zatim je u smešu dodat vodeni rastvor CuSO4 (28 procenata, 25 ml) i reakcija je refluksovana 10 minuta. Nakon reakcije, smjesa je ohlađena, talog je filtriran i ispran ledeno hladnom vodom da bi se dobio ciljni proizvod.
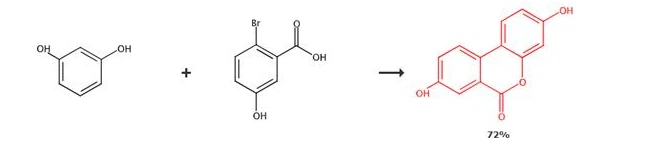
Urolitin A je prirodni proizvod koji se metabolizira u ljudskom tijelu flavonoidnim bojama kao što su trešnje i orasi u biljkama. Trenutno se još uvijek istražuje i razvija laboratorijska metoda sinteze urolitina A, tako da ne postoji jednostavan i rutinski put sinteze.
Korak 1: Sinteza 2,6-dimetoksibenzaldehida (2,6-dimetoksibenzaldehida):
p-metoksibenzil alkohol plus PBr3→ 2,6-dimetoksibenzaldehid
2,6-Dimetoksibenzil alkohol se može dobiti reakcijom p-metoksibenzil alkohola sa fosfornim tribromidom (PBr3). Zatim se p-metoksibenzil alkohol može pretvoriti u 2,6-dimetoksibenzaldehid reakcijom oksidacije.
Korak 2: Sinteza 2-Hidroksi-5-metoksibenzaldehida (2-Hidroksi-5-metoksibenzaldehida):
2,6-dimetoksibenzaldehid plus NaOH → 2-hidroksi-5-metoksibenzaldehid
2-Hidroksi-5-metoksibenzaldehid se može dobiti reakcijom 2,6-dimetoksibenzaldehida sa rastvorom natrijum hidroksida (NaOH).
Korak 3: Sinteza 2-Hidroksi-5-metoksibenzojeve kiseline (2-Hidroksi-5-metoksibenzojeve kiseline):
2-Hidroksi-5-metoksibenzaldehid plus razrijeđena kiselina → 2-hidroksi-5-metoksibenzojeva kiselina
Oksidacijom 2-hidroksi-5-metoksibenzaldehida sa razrijeđenom kiselinom, može se dobiti 2-hidroksi-5-metoksibenzojeva kiselina.
Korak 4: Sinteza 2-bromo-5-hidroksibenzojeve kiseline (2-bromo-5-hidroksibenzojeve kiseline):
2-Hidroksi-5-metoksibenzojeva kiselina plus Br2→ 2-bromo-5-hidroksibenzojeva kiselina
2-Brom-5-hidroksibenzojeva kiselina se može dobiti bromiranjem 2-hidroksi-5-metoksibenzojeve kiseline.
Korak 5: Sinteza urolitina A:
2-bromo-5-hidroksibenzojeva kiselina plus C6H5(OH)2→ urolitin A
Urolitin A se može dobiti reakcijom 2-bromo-5-hidroksibenzojeve kiseline sa resorcinolom u vodenom rastvoru NaOH. Specifični uvjeti reakcije i operativni detalji mogu zahtijevati detaljnije studije i eksperimente za utvrđivanje.
Konverzija aplikacije:
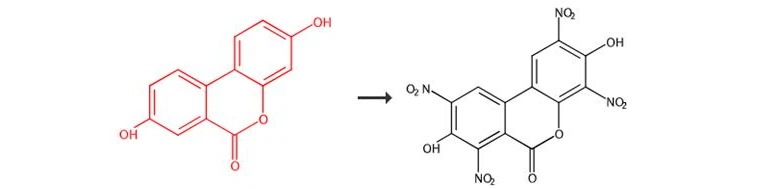
U rastvor urolitina A u AcOH (25 ml) dodata je dušična kiselina (65 procenata, 0.83 g, 13,2 mmol) i dobijena smeša je zagrevana na 50 stepeni 4 sata, a primećena je TLC (EtOAc/n-heksan/MeOH, 7:2:1) za praćenje toka reakcije. Nakon reakcije, rastvarač je uparen pod sniženim pritiskom, a rezultirajući ostatak je rekristaliziran s octenom kiselinom da se dobije 3,8-dihidroksi-2,4,7,9-tetranitro {{18 }}H-Dibenzo[b,d]piran-6-jedan.
Eriodiktiol može biti izoliran iz biljaka, direktno sintetiziran ili polusintetiziran iz hesperidina. Polusintetski eridiktiol se dobija hidrolizom i demetilacijom hesperidina. Metoda koristi hesperidin kao sirovinu, nakon što je hidroliziran kiselom vodenom otopinom glikolne kiseline, dodavanjem bezvodnog aluminij klorida za demetilaciju da bi se dobio eridiktiol, nedostatak je što se u polusintetizirani eridiktiol lako unose nekontrolisane nečistoće, a tokom procesa reakcije vodena voda je teško rukovati. Konkretni koraci su sljedeći:
(1) Osušite kožu slatkovodnog kestena na zraku, usitnite je i ostavite na stranu; po težini, uzmite 1 dio praha od kože vodenog kestena, dodajte ga u rezervoar za ekstrakciju, svaki put dodajte 4-10 dijelova 70% zapreminskog vodenog rastvora acetona i ekstrahirajte na 25 stepeni Potopite 24 sata, potopite 3 puta, filtrirati, sjediniti filtrate, koncentrirati pod sniženim pritiskom u pastu i dobiti ekstrakt.
(2) Po masi, 1 dio ekstrakta se disperguje u 5 dijelova vode da se dobije suspenzija, ekstrahuje 3 puta etil acetatom od 1-2 puta zapremine vode, kombinovani ekstrakti se koncentrišu do suha pod smanjenim pritisak da se dobiju ekstrakti.
(3) Dodajte metanol u ekstrakt dok se potpuno ne otopi, pomiješajte uzorak sa poliamidom 2-4 puta mase ekstrakta, isparite metanol do suhog, napunite kolonu, povežite na MCI kolonu za odvajanje srednjeg pritiska i koristiti 40-100 postotak zapremine Procenat vodenog rastvora metanola se koristi za gradijent eluiranja mobilne faze i detektuje se tankoslojnom hromatografijom. Eluat sa kombinovanom koncentracijom mobilne faze od 65-69 posto po zapremini se sakuplja i koncentrira pod sniženim pritiskom da se dobije sirovi proizvod A.
(4) Dodajte metanol sirovom proizvodu A dok se potpuno ne otopi, pomiješajte uzorak sa 2-4 puta masom poliamida, isparite metanol do suhog, prebacite u poliamidnu kolonu radi odvajanja i koristite zapreminski omjer od 6 :1-3: 1 u rastvoru hloroform-metanol i detektovan tankoslojnom hromatografijom, eluat koji sadrži eridiktiol je sakupljen i kombinovan, i koncentrisan pod sniženim pritiskom da bi se dobio sirovi proizvod B.
(5) Po težini, 1 dio sirovog proizvoda B je otopljen u 4-8 dijelova metanola, a ekvivalentna zapremina metanola se dodaje da se dobije suspenzija, pročišćena hromatografskim gelom Sephadex LH-20 kolonu i eluiran metanolom, detekcija tankoslojnom hromatografijom, sakupljanje i kombinovanje eluata koji sadrži eridiktiol, i koncentriranje pod sniženim pritiskom da se dobije sirovi proizvod C.
(6) Dobijeni sirovi proizvod C se rekristalizira u vodenom rastvoru metanola ili vodenom rastvoru etanola, osuši i dobije eriodiktiol čiji sadržaj dostiže više od 95 procenata.

